Đánh giá hiệu quả xử lý sulfua và crom trong nước thải thuộc da bằng phương pháp hóa học
MỞ ĐẦU
Nước thải từ quá trình thuộc da có độ màu cao, hàm lượng chất rắn lơ lửng (SS) và tổng chất rắn (TS) lớn, hàm lượng các chất hữu cơ cao. Thời gian xả nước thải giữa các công đoạn liên tiếp nhau thường rất dài (12 -24 giờ). Ngoài rahàm lượng sulfua (công đoạn tẩy lông) và Crom (III) (công đoạn thuộc Crom) trong dòng thải hỗn hợp thường cao hơn nhiều lần ngưỡng giới hạn để có thể sử dụng phương pháp sinh học để xử lý nước thải. Do đó áp dụng phương pháp hóa học đểkhử sulfua có trong nước thải của công đoạn tẩy lông ngâm vôi và Crom có trong nước thải từ công đoạn thuộc Crom được xem phương pháp xử lý tối ưu.
Đối với khử sulfua thì nhiều chuyên gia trong ngành đã đánh giá phương pháp oxy hóa dùng oxy không khí có sử dụng xúc tác là phương pháp đơn giản, hiệu quả và chi phí thấp nhất. Sau đó là phương pháp đông keo tụ với phèn sắt. Cụ thể vào năm 1991, Mesdaghinia A. R. và Yousefi Z. (Iran) đã nghiên cứu sử dụng oxy trong không khí để oxy hóa sulfua trong nước thải thuộc da với xúc tác MnSO4 và NiSO4 [5]. Phương pháp này đã được Hiệp hội Nghiên cứu công nghiệp da thuộc Vương quốc Anh (British Leather Manufacturer Research Association) áp dụng trong xử lý nước thải thuộc da.
Còn để xử lý lượng Crom trong nước thải thuộc Crom thì phần lớn các nghiên cứu đều thực hiện theo hướng kết tủa Crom ở dạng hydroxyt [Cr(OH)3] để thu hồi tái sử dụng. Các hóa chất được sử dụng để kết tủa Crom gồm: NaOH, NaHCO3, Na2CO3, Ca(OH)2, Mg(OH)2, MgO. Năm 2001, tác giả Beleza V. M. (Bồ Đào Nha) đã nghiên cứu động học của quá trình khử Crom trong nước thải thuộc da bằng bùn thải của quá trình sản xuất acetylen (gọi tắt là bùn acetylen) [2]. Về bản chất, quá trình này là quá trình kết tủa Crom(III) hydroxyt bằng Ca(OH)2.
Để có thể đánh giá được hiệu quả khử sulfua và crom trong nước thải thuộc da bằng các phương pháp hóa học nhóm nghiên cứu đã tiến hành các thí nghiệm để đánh giá, kiểm chứng và lựa chọn những điều kiện thích hợp nhất để có thể áp dụng được trong xử lý nước thải thuộc da ở Việt Nam.
1. THỰC NGHIỆM
1.1. Đối tượng nghiên cứu
Nước thải của quá trình thuộc da được lấy từ Xưởng thực nghiệm thuộc da – Viện Nghiên cứu Da – Giầy. Nước thải nghiên cứucó thành phần như bảng 1
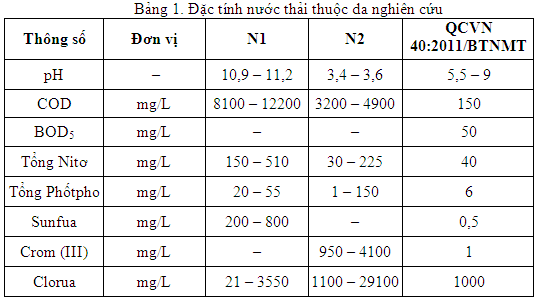
Trong đó:
– NT1: Nước thải từ công đoạn tẩy lông ngâm vôi;
– NT2: Nước thải từ công đoạn thuộc Crom.
1.2. Phương pháp phân tích
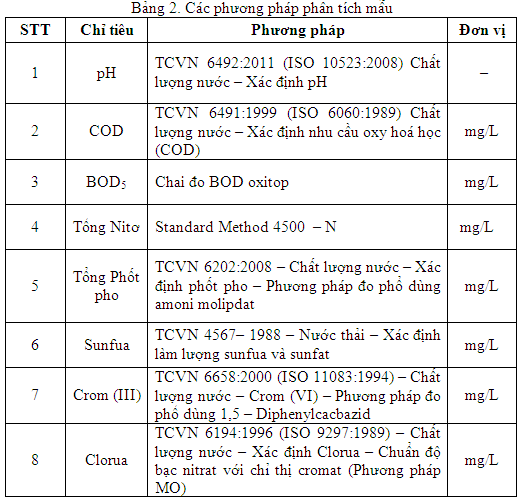
1.3. Phương pháp tính toán kết quả
Hiệu quả xử lý các thông số được tính bằng công thức
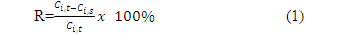
Trong đó: Ci,t: nồng độ của thông số trước khi xử lý
Ci,s: nồng độ của thông số sau khi xử lý
2. KẾT QUẢ THỰC NGHIỆM
2.1. Nghiên cứu khử sulfua trong nước thải tẩy lông ngâm vôi
Quá trình khử sulfua có thể được thực hiện theo 2 hướng: kết tủa với muối sắt (FeSO4 và FeCl3) và oxy hóa bằng oxy không khí. Đây là 2 phương pháp đơn giản, rẻ tiền, được đề cập đến trong nghiên cứu của một số tác giả trên thế giới.
2.1.1. Nghiên cứu khử sulfua bằng phương pháp kết tủa với muối sắt
Cơ sở nghiên cứu:
Về mặt hóa học, ion Fe2+ và Fe3+ có thể phản ứng với ion S2- tạo thành kết tủa FeS hoặc Fe2S3 màu đen theo các phản ứng sau [5]:
Fe2+ + S2- → FeS ↓ (2)
2Fe3+ + 3S2- → Fe2S3 ↓ (3)
Bằng cách sử dụng dư muối sắt hoặc bổ xung chất keo tụ, các kết tủa này có thể lắng xuống đáy thiết bị và tách ra khỏi nước thải.
Theo tính toán từ phương trình (2) và (3), để kết tủa hoàn toàn sulfua trong 1L nước thải thì lượng Fe2+ và Fe3+cần thiết tương ứng là 1.120 mg/L và 747 mg/L (hay FeSO4 và FeCl3 cần thiết tương ứng là 3.040 mg/L và 2.168 mg/L). Nước thải được điều chỉnh pH về khoảng 8 – 8,5 bằng dung dịchH2SO4 1N. Để hạn chế lượng H2S hình thành trong quá trình điều chỉnh pH, lượng axit cần thiết được xác định và kiểm tra trước khi làm thí nghiệm; trong quá trình thí nghiệm, muối sắt được bổ sung ngay sau khi điều chỉnh pH.
Điều kiện tiến hành thí nghiệm:
+ Sulfua S2- = 640 mg/L
+ Tốc độ khuấy là 150 – 200 vòng/phút, thời gian khuấy là 2 phút
+ Liều lượng Fe2+ khảo sát lần lượt là: 750, 1000, 1250 và 1750 mg/L (lượng FeSO4 tương ứng là 2036, 2714, 3393 và 4750 mg/L).
+ Liều lượng Fe3+ khảo sát lần lượt là: 250, 500, 750 và 1000 mg/L (lượng FeCl3tương ứng là 725, 1451, 2175 và 2902 mg/L).
Thí nghiệm còn khảo sát ảnh hưởng của chất keo tụ PAC và chất trợ keo tụpolymer A101 tới hiệu quả lắng của kết tủa. Liều lượng PAC lần lượt là 1250 và 1750 mg/L; liều lượng A101 lần lượt là 0,0025 và 0,005 mg/L.
Kết quả thí nghiệm cho thấy, ở các nồng độ muối sắt khác nhau, kết tủa sắt sulfua hoàn toàn không thể lắng được, ngay cả khi thời gian lắng kéo dài đến 24 giờ. Việc bổ sung PAC hay PAC kết hợp với A101 không giúp tăng khả năng lắng của kết tủa.So sánh với các nghiên cứu của Ignacio Garrote J. [3], Song Z. [6] hay Lofrano G.[4] thì hàm lượng sulfua trong mẫu nước thải lấy tại Viện Nghiên cứu Da Giầy cao hơn khoảng 2,5 – 6,5 lần. Nếu tính toán theo các nghiên cứu trên thì cần phải thực hiện quá trình keo tụ 6 lần hoặc pha loãng nước thải 6 lần để khử hoàn toàn sulfua. Điều này không khả thi về mặt kinh tế và chứa nhiều rủi ro về mặt kỹ thuật.Vì vậy, giải pháp sử dụng phèn sắt (FeSO4 và FeCl3) để khử sulfua trong nước thải tẩy lông ngâm vôi là không khả thi.
2.1.2. Kết quả nghiên cứu khử sulfua bằng quá trình oxy hóa dùng oxy trong không khí với xúc tác MnSO4
Cơ sở nghiên cứu:
Ở nhiệt độ thường, H2S bị oxy hóa chậm bởi oxy không khí tạo thành lưu huỳnh theo phản ứng:
2H2S + O2 → 2S + 2H2O (4)
Phản ứng này cũng có thể xảy ra trong dung dịch nước. Thế khử chuẩn của cặp S/H2S = + 0,14 V, vì vậy về nguyên tắc mọi cặp oxy hóa khử khác có thế khửlớn hơn 0,14 V đều có thể oxy hóa H2S thành lưu huỳnh. Thế oxy hóa khử chuẩn của cặp O2/H2O = 1,229 V (> 0,14 V) [1].
Nếu dư oxy, lưu huỳnh tiếp tục được chuyển hóa thành H2SO3 và H2SO4 do thế khử chuẩn của cặp S/H2SO3 = – 0,45 V, còn cặp SO32-/SO42- = – 0,93 V [1]. Tuy nhiên, quá trình diễn ra chậm do chênh lệch thế oxy hóa không lớn.
Như vậy, cơ chế của quá trình khử sulfua bằng oxy không khí như sau:
2S2- + O2 + 4H+ → 2S + 2H2O (5)
2S + 2O2 + 4OH– → 2SO32- + 2H2O (6)
2SO32- + O2 → 2SO42-(7)
Khi bổ sung xúc tác MnSO4, quá trình khử sulfua tăng lên đáng kể. Trên cơ sở tính chất hóa học của Mangan, biến đổi của xúc tác MnSO4 trong môi trường nước có thể như sau:
MnSO4 → Mn2+ + SO42- (8)
Mn2+ + 2 OH– → Mn(OH)2↓ (9)
4Mn(OH)2 + O2→ 4MnOOH ↓ + 2H2O (10)
Khi đó, phản ứng khử sulfua diễn ra như sau:
2 MnOOH↓ + S2-+ 2 H+ → 2Mn(OH)2 ↓ + S (11)
8MnOOH↓ + S2- + 4H2O → 8Mn(OH)2 ↓ + SO42-(12)
Về bản chất, Mn(OH)2 mới là chất xúc tác cho quá trình khử sulfua trong nước. Ngoài ra, trong môi trường nước, MnSO4 chuyển thành Mn(OH)2 kết tủa, có thể tách ra khỏi nước thải bằng phương pháp lắng thông thường nên không gây ô nhiễm thứ cấp.Thí nghiệm được tiến hành ở 2 lưu lượng khí khác nhau:
-Tại lưu lượng không khí là 0,45 L/L nước thải.phút, điều kiện tiến hành thí nghiệm là:
+ pH = 11,15
+ Hàm lượng S2-= 580 mg/L
+ Liều lượng MnSO4.H2O khảo sát lần lượt là 150, 250 và 350 mg/L.
Hiệu suất khử sunfua được thể hiện qua đồ thị sau:
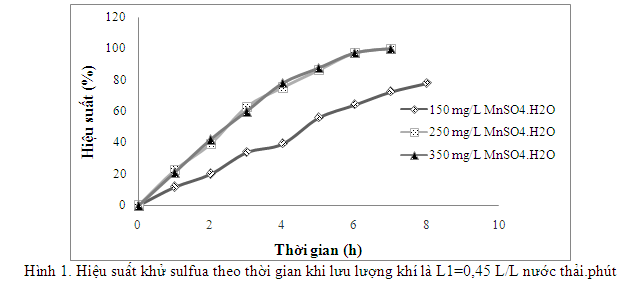
Mối tương quan giữa thời gian cấp khí và hiệu suất khử sulfua được thể hiện trong hình 1 cho thấy ngay sau 1 giờ cấp khí, ở hàm lượng xúc tác MnSO4.H2O là 150 mg/L, hiệu suất khử sulfua đã có sự khác biệt so với ở hàm lượng xúc tác là 250 mg/L. Theo thời gian, sự khác biệt này càng lớn. Sự khác biệt về hiệu suất khử sulfua ở 2 nồng độ xúc tác 250 và 350 mg/L là không đáng kể.
– Tại lưu lượng không khí là 0,9 L/L nước thải.phút, điều kiện tiến hành thí nghiệm là:
+ pH = 11,25
+ Hàm lượng S2-= 656 mg/L
+ Liều lượng MnSO4.H2O khảo sát lần lượt là 200, 300 và 400 mg/L.
Hiệu suất khử sunfua được thể hiện qua đồ thị sau:
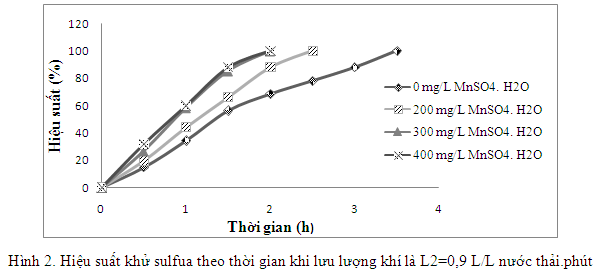
Từ hình 2 ta thấy khi không có mặt xúc tác MnSO4.H2O, thời gian khử hoàn toàn sulfua trong nước thải là 3,5 giờ, bằng ½ thời gian so với quá trình khử sulfua với lưu lượng khí là 0,45 L/L nước thải.phút và hàm lượng xúc tác MnSO4.H2O là 250 mg/L. Ở hàm lượng xúc tác MnSO4.H2O là 200 mg/L, tốc độ khử sulfua tương đối ổn định theo thời gian; sau 1 giờ cấp khí, hàm lượng sulfua còn 368 mg/L (hiệu suất đạt 43,9%); sau 2 giờ cấp khí, hàm lượng sulfua còn 80 mg/L (hiệu suất đạt 87,8%). Khi tăng hàm lượng xúc tác MnSO4.H2O lên 300 và 400 mg/L, hiệu quả khửsulfua sau 1 giờ cấp khí tăng hơn rõ rệt (từ 14,6 – 15,9%); sau 2 giờ cấp khí, sulfua đã được khử hoàn toàn trong khi ở hàm lượng xúc tác là 200 mg/L chỉ mới đạt 87,8%; tuy nhiên, chỉ 30 phút sau, sulfua cũng được khử hoàn toàn.
Đáng chú ý là trong quá trình thí nghiệm, kết tủa CaSO4 màu trắng xuất hiện ngày càng nhiều chứng tỏ sulfua S2-đã bị oxy hóa hoàn toàn thành SO42- .Các sản phẩm khác như lưu huỳnh tự do, gốc thiosulfat S2O32-, sulfit SO32- là các sản phẩm trung gian hình thành trước khi sulfua S2-bị oxy hóa hoàn toàn thành SO42-
Do sự xuất hiện của CaSO4 nên mẫu trước khi đem phân tích sulfua, phải được lọc để loại bỏ CaSO4.Nước thải tẩy lông ngâm vôi có pH cao (pH = 11 – 12) nên các axit béo có trong nước thải dễ bị xà phòng hóa. Mặt khác, một lượng lớn các axit amin, peptit có sẵn trong da động vật khuếch tán vào dòng thải tạo thành các chất hoạt động bềmặt và làm thay đổi sức căng bề mặt của nước. Vì vậy, khi sục khí, lượng bọt hìnhthành lớn. Để tránh bị tràn, phải sử dụng chất khử bọt trong quá trình xử lý. Tuy nhiên, bổ sung chất khử bọt cũng đồng nghĩa với việc đưa thêm chất ô nhiễm mới vào trong nước thải. Vì vậy, khi lựa chọn chất khử bọt cần ưu tiên sửdụng các sản phẩm có thể phân hủy sinh học được và liều lượng sử dụng nhỏ.
Kết quả nghiên cứu cho thấy, tốc độ oxy hóa sulfua phụ thuộc vào 2 yếu tốchính:
– Lưu lượng không khí cấp
– Hàm lượng xúc tác MnSO4.H2O.
Khi tăng lưu lượng không khí, lượng oxy ở dạng hòa tan trong nước thải tăng, làm cho thế oxy hóa khử của oxy tăng lên, phản ứng theo chiều thuận được thúc đẩy và tốc độ của quá trình khử sulfua tăng. Tuy nhiên, lưu lượng không khí không thể tăng lên quá cao do:
+ Hàm lượng oxy hòa tan không thể vượt ngưỡng giới hạn tương ứng với nhiệt độ của nước thải. Khi đạt ngưỡng bão hòa, lưu lượng không khí có thể tăng thêm nữa nhưng hàm lượng oxy hòa tan không thay đổi, tốc độphản ứng đạt tối đa
+ Lưu lượng không khí quá cao có thể thúc đẩy quá trình phát tán muối sulfua, hơi nước và các chất dễ bay hơi khác vào môi trường xunh quanh gây ô nhiễm môi trường.
+ Lưu lượng không khí cao đòi hỏi máy nén khí có công suất lớn, tiêu thụđiện năng tăng, chi phí xử lý cao…
Khi tăng lưu lượng không khí, cần cân đối giữa các yếu tố như hiệu quả khửsulfua theo thời gian, tiêu thụ điện năng và chi phí đầu tư cho máy nén khí.
Hình 2 cũng cho thấy: với hàm lượng sulfua là 656 mg/L, khi không có mặt xúc tác MnSO4 và lượng không khí cấp đủ lớn thì thời gian khử hoàn toàn sulfua không quá dài (3,5 giờ). Như vậy, có thể oxy hóa sulfua bằng oxy không khí mà không cần phải sử dụng xúc tác.
Phương án công nghệ này có ưu điểm là:
– Quy trình công nghệ đơn giản, dễ vận hành
– Chi phí xử lý thấp do không sử dụng xúc tác
– Hoàn toàn không gây ô nhiễm thứ cấp.
Tuy nhiên, để rút ngắn thời gian phản ứng, nâng cao hiệu quả khử sulfua, có thể sử dụng xúc tác là MnSO4.H2O ở nồng độ 200 mg/L kết hợp cấp khí với lưu lượng 0,9 L/L nước thải.phút.
2.2. Nghiên cứu khử Crom trong nước thải thuộc Crom
Crom trong hóa chất thuộc chủ yếu là dạng Crom (III), có thể bị kết tủa ở dạng Crom (III) hydroxyt Cr(OH)3 theo phản ứng:
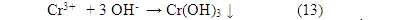
Trong quá trình nghiên cứu, chúng tôi sử dụng một số tác nhân như: MgO, Ca(OH)2, NaOH, NaOH kết hợp với A101, vôi kết hợp với A101, hỗn hợp MgO và vôi.
Các tiêu chí để đánh giá hiệu quả khử Crom là: liều lượng cần thiết để kết tủahoàn toàn Crom, khả năng lắng của kết tủa và dung tích kết tủa.
2.2.1. Nghiên cứu lựa chọn tác nhân kết tủa Crom:
Thí nghiệm được tiến hành với nước thải có:
+ pH = 3,63
+ Hàm lượng Crom: 4097 mg/L
+ Tốc độ khuấy: 160 – 190 vòng/phút
+ Thời gian khuấy: 10 phút
+ Chất trợ keo tụ được bổ sung trước khi dừng khuấy 30 – 45 giây
Sau đó để lắng tự nhiên trong 2 giờ và lấy mẫu phân tích.
Hóa chất kết tủa được bổ sung với liều lượng khác nhau:
+ NaOH: 2,5 – 3,75 – 5,0 – 6,25 và 7,5 g/L
+ 5 g/L NaOH kết hợp dung dịch A101 0,05% với liều lượng lần lượt là 0,025 – 0,075 – 0,125 – 0,250 – 0,375 mg/L
+ Ca(OH)2: 5,0 – 7,5 – 10 – 12,5 – 15 g/L
+ Ca(OH)2: 5,0 – 7,5 – 10 – 12,5 – 15 g/L kết hợp với A101 0,05 mg/L
+ MgO: 5,0 – 7,5 – 10 – 12,5 – 15 g/L
+ Hỗn hợp 10% (MgO/vôi = ¼): 5,0 – 7,5 – 10 – 12,5 – 15 g/L.
Kết quả thực nghiệm cho thấy: khi kết tủa Crom bằng vôi, NaOH và NaOH kết hợp A101 thì sau 2 giờ lắng tự nhiên, thể tích bùn rất lớn (> 90% với vôi và với NaOH bùn hầu như không lắng). Thậm chí, sau 24 giờ lắng tự nhiên, bùn vẫn còn chiếm khoảng 90%. Như vậy, vôi, NaOH hay NaOH kết hợp với A101 có thể kết tủa được Crom nhưng bông keo tụ xốp, tỷ trọng nhỏ nên rất khó lắng. Vậy vôi, NaOH hay NaOH kết hợp với A101 là không phù hợp để khử Crom trong nước thải thuộc Crom.
Với các tác nhân kết tủa là Ca(OH)2, MgO và hỗn hợp MgO/vôi (tỷ lệ ¼), hiệu quả khử Crom và liều lượng các tác nhân kết tủa được trình bày trong hình 3.
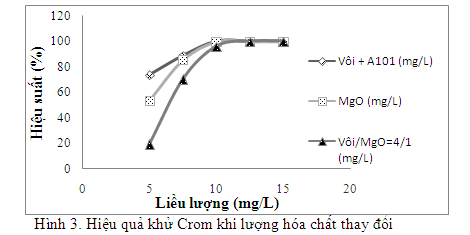
Hình 3 biểu diễn mối tương quan giữa hiệu quả khử Crom và liều lượng chất kết tủa cho thấy: ban đầu, tại liều lượng 5 g/L, khoảng cách giữa các đường hiệu suất là rất rõ ràng. Nhưng khi tăng liều lượng sử dụng, khoảng cách giữa các đường hiệu suất nhanh chóng được thu hẹp, đến liều lượng > 12,5 g/L thì hiệu suất khử Crom bằng các tác nhân khác nhau đều đạt 100%. Kết quả thí nghiệm cho thấy: để khử hoàn toàn Crom trong 1L nước thải cần 10 gam MgO hoặc 10 g vôi kết hợp với 0,05 mg A101. Kết quả thí nghiệm này cũng phù hợp với tính toán lý thuyết (8,6 g vôi cho 1 lít nước thải). Đối với hỗn hợp vôi/MgO, để khử hoàn toàn Crom trong 1L nước thải cần 10 gam vôi và 2,5 gam MgO. So với kết quả ở trên thì MgO chỉ có tác dụng giúp tăng khả năng lắng của bùn tương tự A101 trong khi chi phí khi sử dụng MgO cao hơn so với A101. Do đó, trong thí nghiệm tiếp theo là khảo sát khả năng lắng của bùn, chúng tôi chỉ sửdụng 2 tác nhân kết tủa là MgO và vôi kết hợp với A101.
2.2.2. Khảo sát khả năng lắng của bùn
Thí nghiệm khảo sát khả năng lắng của bùn được thực hiện với nước thải:
+ pH = 3,34
+ Hàm lượng Crom = 4090 mg/L
+ Tốc độ khuấy: 160 – 190 vòng/phút
+ Thời gian khuấy: 10 phút
+ 9 g/L MgO
+ 9 g/L vôi kết hợp với A101 có nồng độ 0,05 – 0,10 – 0,20 mg/L
Sau quá trình keo tụ, hỗn hợp được chuyển sang ống đong 500 mL để khảo sát thể tích bùn. Kết quả khảo sát được trình bày như trong hình 4.
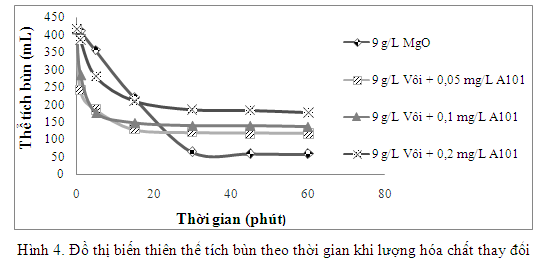
Biến thiên thể tích bùn trong hình 4 cho thấy: khi sử dụng vôi kết hợp A101, quá trình lắng diễn ra nhanh trong khoảng 20 phút đầu tiên (đường biến thiên thể tích có độ dốc rất lớn), sau đó thể tích bùn ít biến đổi (đường biến thiên thể tích gần như nằm ngang). Khi kết tủa bằng MgO, tốc độ lắng của bùn chậm hơn nhưng ổn định, sau thời gian 30 phút thì thể tích bùn ít biến đổi. Khi sử dụng lượng A101, kích thước bông bùn tăng, bùn trở nên xốp hơn làm thể tích bùn tăng. Ngoài ra, do kích thước bông bùn lớn nên xuất hiện hiện tượng “lắng chen” giữa các bông bùn làm giảm tốc độ lắng của bông bùn.
Như vậy, quá trình khử Crom trong nước thải thuộc Crom có thể được thực hiện bằng phương pháp kết tủa, trong đó MgO là chất kết tủa tốt nhất. Điều này giống với kết luận của nhiều nghiên cứu trên thế giới cụ thểWang Weixiao (Trung Quốc) [7] cho rằng có thể sử dụng NaOH để kết tủa Crom nếu sử dụng thêm PAM (Polyacrylamide hay PAA). Tuy nhiên, kết quả thực nghiệm cho thấy NaOH không phải là chất kết tủa thích hợp. Đáng chú ý là lượng PAM mà Weixiao sử dụng không nhỏ: 2,5 – 4 kg PAM/m3 nước thải.
Nếu xét về kinh tế thì sử dụng vôi kết hợp với A101 sẽ tốt hơn do liều lượng vôi và MgO cần thiết là tương đương nhau trong khi giá vôi thương mại chỉ bằng khoảng 1/5 so với giá của MgO. Lượng A101 cần thiết khi kết tủa bằng vôi là không lớn: 1 m3 nước thải cần 5 g A101 (nhỏ hơn gần 1000 lần so với nghiên cứu của Weixiao [7]).
Khi lượng A101 tăng thì tốc độ lắng giảm, thể tích bùn tăng. Điều này chứng tỏ A101 là cầu nối giữa các kết tủa Crom hydroxyt rất tốt nhưng khi sử dụng với liều lượng lớn, mật độ kết tủa cao, bông bùn có kích thước lớn và xốp hơn, xuất hiện sự cản trở lẫn nhau giữa các bông bùn trong quá trình lắng.
Tóm lại, để tách Crom trong nước thải thuộc Crom, có thể dùng vôi với chất trợ lắng A101 để kết tủa. Ở Việt Nam, vôi là nguyên liệu sẵn có, giá thành rẻ.
3. KẾT LUẬN
Sau khi tiến hành nghiên cứu xử lý khử sulfua trong nước thải tẩy lông ngâm vôi và khử Crom trong nước thải thuộc Crom của nước thải thuộc da nhóm tác giả nhận thấy:
Đối với nghiên cứu khử sulfua trong nước thải tẩy lông ngâm vôi
– Phương pháp kết tủa bằng muối sắt: do nước thải tẩy lông ngâm vôi có hàm lượng sulfua rất cao (580 – 656 mg/L) nên phương pháp kết tủa bằng muối sắt là không khả thi về mặt kỹ thuật
– Phương pháp oxy hóa dùng oxy của không khí: ngay cả khi hàm lượng sulfua khá lớn (656 mg/L), chỉ sau 3,5 giờ cấp khí liên tục với tỷ lệ 0,9 L/L nước thải.phút, sulfua đã được khử hoàn toàn. Để rút ngắn thời gian oxy hóa, quá trình oxy hóa bằng oxy của không khí có thể kết hợp bổ sung xúc tác là MnSO4.H2O. Kết quả cũng cho thấy: ở hàm lượng MnSO4.H2O là 250 mg/L và lưu lượng khí là 0,45 L/L nước thải.phút trong 7 giờ hay ở hàm lượng 300 mg/L MnSO4.H2O và lưu lượng khí là 0,9 L/L nước thải.phút trong 2 giờ, sulfua đã được khử hoàn toàn.
Đối với nghiên cứu khử Crom trong nước thải thuộc Crom:
Phương pháp kết tủa hóa học được áp dụng trong nghiên cứu khử Crom trong nước thải thuộc Crom. Các tác nhân kết tủa được sử dụng là: NaOH, NaOH kết hợp với A101, Ca(OH)2, Ca(OH)2 kết hợp với A101, MgO và hỗn hợp MgO/Ca(OH)2 (tỷ lệ ¼).
Kết quả nghiên cứu lựa chọn các tác nhân kết tủa cho thấy:
+ Do hàm lượng Crom quá cao (4097 mg/L) nên NaOH, NaOH kết hợp với A101 và Ca(OH)2 có thể kết tủa được Crom nhưng bông keo tụ xốp, tỷtrọng nhỏ nên rất khó lắng. Vì vậy, việc tách bùn ra khỏi nước sau xử lý rất khó khăn. Việc sử dụng các tác nhân trên là không khả thi về mặt kỹthuật.
+ Các tác nhân kết tủa Crom có hiệu quả gồm: MgO, Ca(OH)2 kết hợp với A101 và hỗn hợp MgO/Ca(OH)2 (tỷ lệ ¼).
– Kết quả nghiên cứu hiệu quả kết tủa Crom của MgO, Ca(OH)2 kết hợp với A101 và hỗn hợp MgO/Ca(OH)2 (tỷ lệ ¼) cho thấy:
+ Hiệu quả khử Crom của MgO cao: dung tích bùn tạo ra là nhỏ nhất (chiếm 14,75% thể tích nước thải), để kết tủa hoàn toàn 1 g Crom III trong nước thải cần 2,4 g MgO
+ Ca(OH)2 kết hợp với chất trợ keo tụ A101 cũng cho kết quả khả quan. Với hàm lượng Ca(OH)2 là 10 g/L, Crom trong nước thải ở nồng độ Crom III = 4097 mg/L được kết tủa hoàn toàn. Chất trợ keo tụ A101 giúp tăng khả năng lắng của bùn, liều lượng A101 sử dụng cho 1 m3 nước thải là 2,5 g.
TÀI LIỆU THAM KHẢO
1. Lưu Hữu Thục, Nguyễn Trí Hạnh, Nguyễn Hữu Cường (2001), “Sổ tay kỹ thuật thuộc da”, Viện Nghiên cứu Da Giầy, Hà Nội.
2. V.M.Beleza, R.A.Boaventura, M.F.Almeida (2001), “Kinetics of Chrome Removal from Spent Tanning Liquors Using Acetylene Production Slude”, Environmental Science Technology, 35, p. 4379 – 4383.
3. J.Ignacio Garrote, Manuel Bao, Pablo Castro and Manuel J.Bao (1995), “Treatment of tannery effluents by a two step coagulation/flocculation process”, Water Research, 29(11), p.2605 – 2608.
4. G. Lofrano, V. Gelgiorno, M. Gallo,A. Raimo, S. Meric (2006), “Toxicity reduction in leather tanning wastewater by improved coagulation flocculation process”, Global NEST Journal, 8 (2), p. 151- 158.
5. A.R. Mesdaghinia, Z.Yousefi (1991), “The use of oxygen in catalytic oxidation of sulfide in tannery waste”, Iranian Journal of Public Health, 20 (1 – 4), p. 17 – 25.
6. Z.Song, C.J.William, R.G.J.Edyvean (2001), “Treatment of tannery wastewater by chemical coagulation, Desalination”, 164, p. 249 – 259.
7. Wang weixao, Ha Jing, Li Zhaoyang, Liu kui, Gao Leuhong (2009), “Chromium (III) removal tannery wastewater by precipitator and flocculation – sedimentation”, Chemical Journal on Internet, 14 (3), p. 14
Trần Thị Thu Hiền1, Nguyễn Việt Hùng2, Trần Đức Thảo3
1Khoa Hoá, ĐH Quy Nhơn
2UBND Thị xã Phúc Yên, Tỉnh Vĩnh Phúc
3Khoa CNSH & KTMT, ĐH Công nghiệp Thực phẩm TP.HCM
(Nguồn tin: Vnniosh.vn)
