Xây dựng quy trình kỹ thuật phân tích định lượng PGA (axit Phenylglyoxylic) – sản phẩm chuyển hóa của Ethylbenzen trong nước tiểu bằng phương pháp sắc ký lỏng khối phổ.
I. ĐẶT VẤN ĐỀ
Ethylbenzen là đồng đẳng của benzene, được công nhận là tác nhân gây bệnh nghề nghiệp ở trong nước và trên thế giới, công nghiệp sản xuất styren thì ethylbenzen là nguồn nguyên liệu chính [1].Trong một số ngành công nghiệp khác như sản xuất sơn, điện tử, ethylbenzen luôn lẫn trong những dung môi như benzene, toluen, xylen. Xylen công nghiệp lẫn khoảng 20-40% ethylbenzen [2], trong khi xylen là nguyên liệu chính được sử dụng cho sản xuất sơn và một số ngành công nghiệp khác.
Ở nước ta hiện nay, việc sử dụng ethylbenzen ngày càng phổ biến, nhưng Bộ y tế mới chỉ có quy định về giám sát sinh học choNLĐcó tiếp xúc với benzene, toluene, xylen, chưa có giám sát sinh học cho NLĐcó tiếp xúc với ethylbenzen [3].Nên việc bảo vệ NLĐ có tiếp xúc với ethylebenzen thì chưa được quan tâm một cách thỏa đáng.
Trên thế giới nhiều nước đã sử dụng sản phẩm chuyển hóa của ethylbenzen trong nước tiểu là axit phenylglyoxylic (PGA) làm một trong những chỉ số cho giám sát sinh học đối vớiNLĐ có tiếp xúc với ethylbenzen (theo ACGHI-2018). Ở Việt Nam, quy trình phân tích PGA niệu được công bố rất hạn chế, việctham khảo quy trình phân tíchchất này đối với phòng thí nghiệm tại Việt Nam gặp nhiều khó khăn. Tổng hợp những lý do nêu trên, chúng tôi đặt vấn đề nghiên cứu: “Xây dựng quy trình phân tích PGA (axit phenylglyoxylic) – sản phẩm chuyển hóa của ethylbenzen trong nước tiểu bằng phương pháp sắc ký lỏng khối phổ”, nhằm mục tiêu là: xây dựng được quy trình phân tích PGA trong nước tiểu bằng phương pháp sắc ký lỏng khối phổ với độ chính xác trên 95%, giới hạn định lượng nhỏ hơn 0,1mg/L. Góp phần đề xuất làm chỉ số giám sát sinh học đối vớiNLĐ có tiếp xúc với ethylbenzen .
II. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
2.1. Đối tượng nghiên cứu
Quy trình phân tích PGA niệu-chất chuyển hóa của ethylbenzen trong nước tiểu của người lao động có tiếp xúc nghề nghiệp.
2.2. Phương pháp nghiên cứu
– Tiến hành theo phương pháp nghiên cứu thực nghiệm trong phòng thí nghiệm của Viện khoa học ATVSLĐ bằng cách ứng dụng Phương pháp phân tích được xây dựng theo tài liệu của Laboratory Procedure Manual – The Centers for Disease Control and Prevention (CDC-2012) [4].
– Khảo sát trong phòng thí nghiệm: xây dựng quy trình, phân tích mẫu thực nghiệm
– Lấy mẫu ngoài hiện trường: lấy mẫu nước tiểu của người lao động tại nơi làm việc
2.3. Phương pháp kỹ thuật thực hiện:
2.3.1. Xây dựng quy trình
Thử nghiệm ứng dụng phương pháp phân tích sắc ký lỏng khối phổ với các điều kiện:
– Thiết bị:Máy sắc kýlỏng ba lần tứ cực LC/MA, nhãn hiệu HPLC 1290/MSD6430B của Agilent, Tủ âm sâu 860C,…
– Dụng cụ: Các dụng cụ chuyên dùng như bình định mức, pipet, cột C18 dài 150mm, kích thước hạt 1.8 µm,…
Hóa chất: Hóa chất sử dụng trong đề tài của hãng Sigma đảm bảo độ tinh khiết để phân tích lượng vết như PGA; Ammonium acetate; Methanol; Axit acetic…
Phương pháp phân tích được xây dựng theo tài liệu của Laboratory Procedure Manual – The Centers for Disease Control and Prevention (CDC-2012) [4].
2.3.3. Xác định sản phẩm chuyển hóa
Xác định bằng quy trình xây dựng được trên máy sắc kí lỏng khối phổ của Agilent.
III. KẾT QUẢ VÀ BÀN LUẬN
3.1. Kết quả xây dựng quy trình
3.1.1.Chuẩn hóa các điều kiện cho phép đo
Để chọn được các điều kiện tối ưu cho xây dựng quy trình chúng tôi đã tiến hành khảo sát, đánh giávà thu được kết quả của từng điều kiện như dưới đây.
3.1.1.1.Hóa chất và dung dịch chuẩn
– Hóa chất: PGA; Ammonium acetate; Methanol; Axit aceticcủa Sigma
– Dung dịch chuẩn: pha PGA trong nước cất hai lần để được các nồng độ từ 0,01-8µg/ml.
– Pha động là: 5:Ammonium acetate (10M) – kênh A; 95: Methanol – kênh B
3.1.1.2. Các thông số cài đặt trên máy LC/MS
Đối với mỗi phương pháp các thông số cài đặt trên máy rất quan trọng, nếu một thông số không phù hợp sẽ ảnh hưởng đến chất lượng của kết quả phân tích mẫu. Đề tài tiến hành khảo sát đối với từng thông số và thu được được các giá trị tối ưu. Tại các giá trị này kết quả của phép đo là tốt nhất. Giá trị của các thông số tối ưu cụ thể như sau:
* Điều kiện trên LC
– Tốc độ dòng: 0,2 ml/phút
– Tỉ lệ dung môi: A: 5% B: 95%
– Thời gian chạy mẫu: 4 phút
– Thể tích bơm mẫu: 15 µl
– Nhiệt độ cột: 400C
* Điều kiện MS
– Nguồn tạo ion: ESI
– Năng lượng ion hóa : 70eV
– Chạy chế độ: MRM
– Phổ m/z: 149/77
3.1.2. Chọn các điều kiện lấy mẫu, xử lý mẫu để có dung dịch đo
3.1.2.1. Lấy mẫu
Mẫu nước tiểu được thu vào cuối ca của ngày làm việc cuối tuần. Thu từ 5-10ml nước tiểu đựng vào ống thủy tinh có thể tích 15-20ml, loại ống chịu được điều kiện âm sâu (-800C). Bảo quản lạnh tại hiện trường, khi đưa về phòng thí nghiệm được bảo quản âm sâu trước khi phân tích.
3.1.2.2. Xử lý mẫu
Mẫu được xử lý với nhiều điều kiện khác nhau và đề tài thu được điều kiện cho kết quả tốt nhất là quy trình xử lý mẫu như dưới đây:
Mẫu được pha bằng dung dịch Ammonium acetate (10mM) với tỷ lệ 1 mẫu : 9 Ammonium acetate (10M), lắc đều lọc qua màng lọc 0,2µm.
Dung dịch chuẩn để xây dựng đường chuẩn được xử lý như mẫu phân tích ở các mức nồng độ: 0,01µg/ml; 0,1 µg/ml; 1µg/ml; 2µg/ml; 3µg/ml; 4µg/ml; 5µg/ml.
3.1.3. Đánh giá các điều kiện của quy trình
3.1.3.1. Khảo sát khoảng tuyến tính
* Khảo sát khoảng tuyến tính
Khoảng nồng độ chất phân tích từ giới hạn định lượng đến giới hạn tuyến tính gọi là khoảng tuyến tính. Khoảng tuyến tính của mỗi nguyên tố phân tích ở mỗi vạch phổ khác nhau là khác nhau. Vạch phổ nào có độ hấp thụ càng nhạy thì khoảng tuyến tính càng hẹp[2].
Đề tài tiến hành khảo sát khoảng tuyến tính của PGA bằng cách: pha một dãy chuẩn của PGA trong nước cất hai lầnvới nồng độ là: 0,01 ; 0,05 ; 0,1; 1; 2; 3; 4; 5; 6; 7; 8; 9; 10(µg/mL).
Căn cứ vào kết quả thu được đề tài nhận thấy khoảng tuyến tính phương pháp phân tíchPGA trong nước tiểu là từ LOQ-8µg/mL. Vì vậy khi phân tích mẫu nếu hàm lượng nguyên tố cần phân tích nằm ngoài khoảng tuyến thì phải làm giàu mẫu hoặc pha loãng mẫu để phân tích mới đảm bảo được độ chính xác của phép đo.
* Xây dựng đường chuẩn
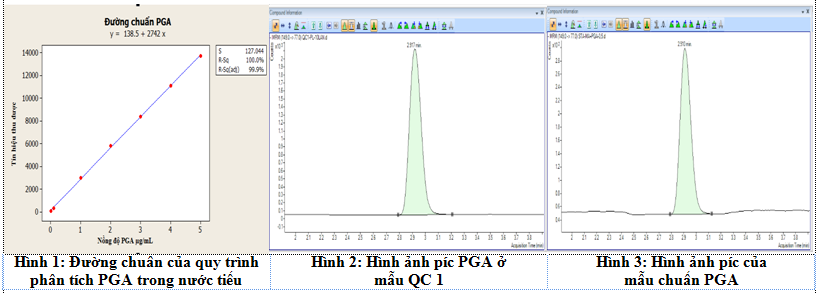
Đường chuẩn
Từ kết quả khảo sát khoảng tuyến tính đề tài sử dụng phần mềm minitab để xây dựng đường chuẩn. Phương trình đường chuẩn của PGA trong nước tiểu được chỉ ra ở dưới đây:
Theo kết quả thu được từ phần mềm minitab 18.0 phương trình hồi quy đầy đủ của đường chuẩn cho phân tích PGA trong nước tiểu có dạng: y =(138±207,04)+ (2742± 7543) x
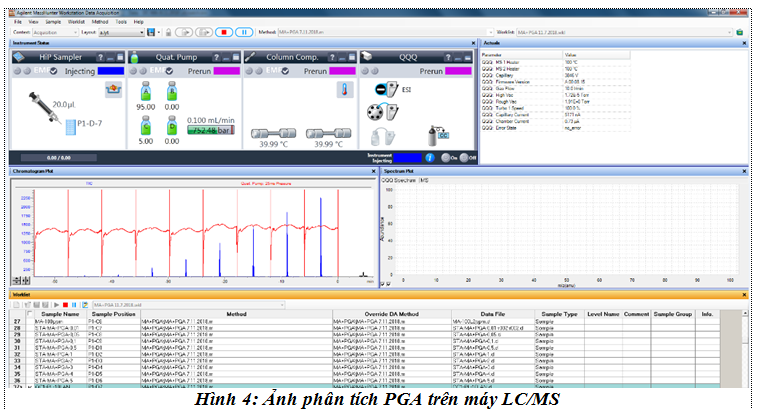
Đánh giá phương trình hồi quy của đường chuẩn
Trong phương trình y = a + bx, trường hợp lý tưởng xảy ra khi a = 0 (khi không có chất phân tích thì không có tín hiệu). Tuy nhiên, trong thực tế các số liệu phân tích thường mắc sai số ngẫu nhiên luôn làm cho a ≠ 0. Nếu giá trị a ≠ 0 có nghĩa thống kê thì phương pháp phân tích sẽ mắc sai số hệ thống. Vì vậy trước khi sử dụng đường chuẩn cho phân tích cần kiểm tra sự khác nhau giữa giá trị a và giá trị 0.
Kiểm tra a với giá trị 0 theo tiêu chuẩn thống kê Fisher (chuẩn F)[2,5].
Nếu Ftính< Fchuẩn (F(0.95; 4; 5)) thì sự sai khác giữa giá trị a và 0 không có ý nghĩa thống kê và ngược lại. Kết quả đánh giácủa đề tàicho thấy Ftính = S’2/S2= 4,25 ; Fchuẩn = F(0,95;4;5) = 5,19 – tức là Ftính< Fchuẩn ở phương trình đường chuẩn phân tích PGAtrong nước tiểu. Có nghĩa là sự sai khác giữa giá trị a và 0 không có ý nghĩa thống kê. Vì vậy phương pháp phân tích trên không mắc sai số hệ thống.
3.1.3.2. Giới hạn phát hiện (LOD), giới hạn định lượng (LQD)
Đối với sắc ký thì việc xác định giới hạn phát hiện (LOD) và giới hạn định lượng (LOQ) dựa theo tỷ số tín hiệu/nhiễu đường nền là khá phổ biến[2]. Đề tài sử dụng cách này để tính LOD, LOQ bằng cách thêm một lượng chất chuẩn nhỏ dần vào mẫu trắng và tại nồng độ 0,001µg/mLthu được tín hiệu cao gấp 3 lần so với tín hiệu đường nền.Như vậy theo phương pháp tính LOD dựa trên tỷ số tín hiệu/nhiễu đề tài thu được LOD=0,001µg/mL, LOQ=0,01µg/mL.
Căn cứ vào kết quả thu được đề tài nhận thấy trong quy trình phân tích PGA trong mẫu nước có giới hạn phát hiện 0,001µg/mL, giới hạn định lượng là 0,01µg/mL. Vậy khoảng tuyến tính của PGAtrong quy trình phân tích PGAniệu là (LOQNước tiểu– 5)µg/mL tương đương (0,01-5)µg/mL.
3.1.3.3. Đánh giá độ chính xác của phương pháp
Theo quan điểm của tiêu chuẩn quốc tế (ISO – 15189) và tiêu chuẩn Quốc gia (TCVN 6910 1- 6:2005) độ chính xác của phương pháp được đánh giá qua độ chụm và độ đúng[5].
– Độ chụm chỉ mức độ giao động của các kết quả thử nghiệm độc lập quanh giá trị trung bình.
– Độ đúng chỉ mức độ gần nhau giữa giá trị trung bình của kết quả thử nghiệm và giá trị thực hoặc giá trị được chấp nhận là đúng.
* Kiểm tra độ chụm
Trong khuôn khổ đề tài đề tài kiểm tra độ chụm bằng cách dùng mẫu thử thêm chuẩn – pha ba loại mẫu có nồng độ thêm chuẩn bằng giá trị gần điểm đầu, điểm giữa, điểm gần cuối của khoảng tuyến tính (tương đương với các mức nồng độ thấp, trung bình, cao). Mỗi mức nồng độ lặp lại 10 lần. Trên cơ sở kết quả các mẫu lặp lại đề tài đánh giá độ thu hồi theo công thức sau:

Sau đó tính độ thu hồi chung là trung bình của độ thu hồi các lần lặp lại.
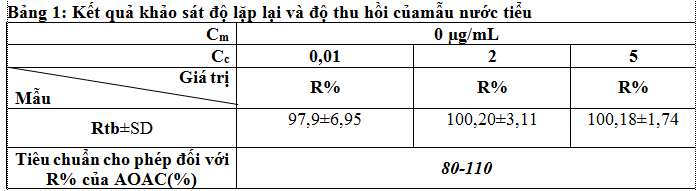
Cm là mẫu nước tiểu không phát hiện PGA; Tại mỗi nồng độ lặp lại 10 lần
Theo tiêu chuẩn của AOAC với khoảng nồng độ từ 0,01-10µg/mL hiệu suất thu hồi cho phép là từ 80-110%. Kết quả ở bảng trên cho thấy hiệu suất thu hồi của quy trình phân tích tốt, nằm trong tiêu chuẩn cho phép. Điều đó chứng tỏ độ chụm của phương pháp đạt yêu cầu.
* Kiểm tra độ đúng
Có nhiều cách để đánh giá độ đúng của phương pháp. Trong nghiên cứu này chúng tôi đã sử dụng mẫu chuẩn để đánh giá độ đúng của quy trình phân tích. Mẫu chuẩn hay còn gọi là vật liệu chuẩn – là mẫu phân tích có hàm lượng đã được xác định trước và đúng. Có nhiều cấp vật liệu chuẩn khác nhau, trong đó cao nhất là CRM (Certified reference materials – mẫu chuẩn được chứng nhận) được cung cấp bởi các tổ chức có uy tín trên thế giới (RECIPE – của Đức). Kết quả phân tích mẫu CRM thể hiện qua bảng sau
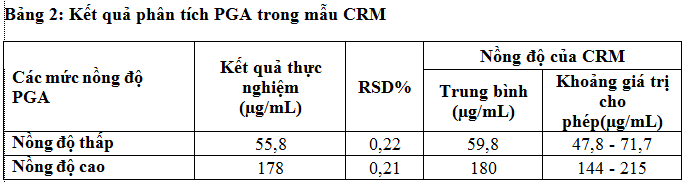
Từ Bảng 2 ở trên đề tài nhận thấy kết quả phân tích mẫu CRM cho các giá trị nằm trong khoảng giá trị cho phép và có giá trị gần sát với giá trị trung bình của mẫu CRM. Ở mức nồng độ thấp nồng độ thu được là 55,8(µg/mL) xấp xỉ giá trị trung bình của mẫu CRM (59,8 µg/mL) và thuộc khoảng giá trị cho phép là (47,8 – 71,7µg/mL). Tương tự, ở mức nồng độ cao các giá trị thu được đều nằm trong khoảng cho phép, giá trị trung bình thu được là 178 xấp xỉ giá trị trung bình của mẫu CRM (180µg/mL)và cũng thuộc khoảng giá trị cho phép là (144 – 215µg/mL). Điều đó chứng tỏ phương pháp phân tích đảm bảo độ đúng.
Từ kết quả kiểm tra độ chụm và độ đúng của phương pháp cho thấy phương pháp mà đề tài khảo sát đảm bảo độ chính xác.
3.1.3.4. Đánh giá độ ổn định của phương pháp
Đánh giá độ ổn định của phương pháp có thể sử dụng mẫu CRM, khi không có mẫu CRM thì có thể sử dụng (chuẩn F) hoặc (chuẩn t) để đánh giá hai nhóm kết quả trong 2 điều kiện [5], [6]. Trong nghiên cứu này để kiểm tra độ ổn định của phương pháp đề tài tiến hành với mẫu CRM khi thay đổi điều kiện về thời gian phân tích kết quả thu được như sau:
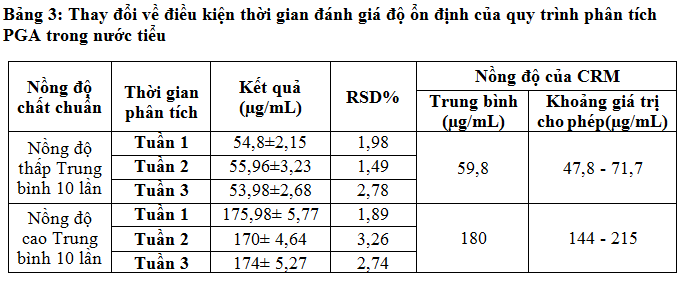
Với điều kiện thay đổi về thời gian, độ ổn định của phương pháp vẫn đảm bảo. Kết quả đánh giá được thể hiện ở Bảng 3. Qua 3 tuần – với các thời điểm phân tích khác nhau kết quả mẫu CRM thu đượcđều nằm trong khoảng giới hạn cho phép và ở các mức nồng độ giá trị thu được luôn gần với giá trị trung bình cho trước của mẫu CRM.
Như vậy, qua việc đánh giá những tiêu chí cần thiết cho một quy trình phân tích,đề tài nhận thấy quy trình phân tích PGA trong nước tiểu bằng phương pháp sắc ký lỏng khối phổ của đề tài là đạt yêu cầu của một quy trình phân tích.
Từ quy trình trên đề tài có một số nhận xét như sau:
Quy trình của nhóm có khoảng tuyến tính, giới hạn phát hiện và giới hạn định lượng tương đương, thậm chí còn tốt hơn một số quy trình phân tích của một số tác giả khác.
Cụ thể so với phương phápcủa S.C.Chua và cộng sự [7] phân tích trên máy sắc ký lỏng hiệu năng cao (HPLC) cóLODPGA = 0,5µg/mlthì LOD của đề tài tốt hơn nhiều (0,001µg/ml).Nghiên cứu của S.W.Cui và cộng sự [8] phân tích trên máy GC/MS có LOD = 1,1 µg/ml, LOQ là 3,7 µg/ml – cao hơn nhiều so với LOD, LOQ của đề tài. Đặc biệt so với phương pháp của CDC mà đề tài đã tham khảo [4] – quy trình phân tích cũng trên thiết bị sắc ký lỏng khối phổLC/MS/MS, LOD của phương pháp này là 0,012µg/ml – cao hơn nhiều so với LOD của đề tài xây dựng được. Phương pháp của CDC có khoảng tuyến tính 0,012- 0,806µg/ml, hẹp hơn so với khoảng tuyến mà đề tài thu được (0,01-5µg/ml), và hiệu suất thu hồi (97,9 – 100,2%), độ chính xác trên 97,5% tương đương với phương pháp của CDC và tốt hơn của S.C.Chua và cộng sự [7] – có hiệu suất thu hồi là 84%, cũng như phương pháp của S.W. Cui và cộng sự (2017) [8] có hiệu suất thu hồi từ 91,6% – 97,1%.Ngoài ra so với phương pháp của CDC mà đề tài đã tham khảo thì phương pháp phân tích của chúng tôi sử dụng pha động với một kênh có Ammonium acetate (10mM), tiết kiệm hơn so với phương pháp của CDC là Ammonium acetate (15mM).
3.2. Ứng dụng quy trình phân tích
Kết quả phân tích PGA trong nước tiểu của người lao động (NLĐ). Đề tài lấy ngẫu nhiên 90 mẫu nước tiểu NLĐ làm việc tại ở một số công ty sản xuất sơn, tiếp xúc trực tiếp với ethylbenzen, sử dụng quy trình xây dựng được phân tích và cho kết quả như sau:
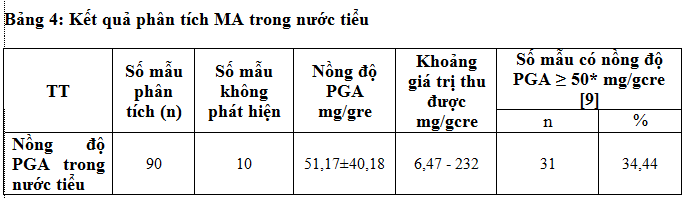
Cre – Creatinin;
* – Theo nghiên cứu của Knecht U và cộng sự tại nồng độ ethylbenzen trong môi trường là 20ppm
(giới hạn cho phép của ethylbenzen) thì nồng độ PGA xấp xỉ 50mg/gcre.
Kết quả Bảng 4 cho thấy: Trong 90 đối tượng tiếp xúc trực tiếp với ethylbenzen được lấy nước tiểu xét nghiệm nồng độ PGA, thì nồng độ trung bình của PGA thu được là 51,17±40,18(mg/gre). Theo nghiên cứu của Knecht U và cộng sự cho thấy tại nồng độ ethylebenzen tối đa cho phép PGA thu được là xấp xỉ 50mg/gcre. Như vậy kết quả trung bình của PGA ở số đối tượng có tiếp xúc trực tiếp với ethylbenzen có giá trị cao hơn giá trị ước tính của PGA tại nồng độ ethylbenzen tối đa cho phép.
Nếu xét trên từng đối tượng thì kết quả có 31 đối tượng (34,44%) có nồng độ PGA ≥ 50mg/gcre. Điều này cho thấy có nhiều người lao động đã tiếp xúc với ethylebenzen vượt tiêu chuẩn cho phép. Ở nước ta hiện nay, nhiễm độc ethylbenzen ở người lao động có tiếp xúc nghề nghiệp đã được công nhận, nhưng lại chưa có giám sát sinh học. Từ kết quả nghiên cứu này chúng tôi nhận thấy nguy cơ ethylbenzen ảnh hưởng đến sức khỏe của người lao động là rất cao. Kết quả này cũng cho thấy người lao động có tiếp xúc với ethylbenzen cần có biện pháp bảo vệ hợp lý và kịp thời để có thể phòng, tránh được bệnh nghề nghiệp.
Sau khi sử dụng quy trình xây dựng được để phân tích mẫu thực, đề tài nhận thấy quy trình ổn định, đảm bảo kết quả chính xác. Chính vì vậy quy trình dự thảo ban đầu không cần thay đổi gì sau khi đề tài áp dụng thực tế.Quy trình này có thể ứng dụng trên các máy thế hệ tương đương hoặc thế hệ tiếp theo của hãng. Đối với những hãng khác nếu là những máy có điều kiện và tính năng kỹ thuật tương tự, hiện đại hơn thì càng tốt đều có thể dùng được.
IV. KẾT LUẬN VÀ KIẾN NGHỊ
4.1. Kết luận
* Xây dựng được quy trình kỹ thuật phân tích định lượng chỉ số axit mandelic(MA) theo phương pháp sắc ký lỏng khối phổvới những thông số cơ bản là: Khoảng tuyến tính: 0,01-8µg/ml; Giới hạn phát hiện: 0,001µg/mL; Giới hạn định lượng: 0,01µg/mL; Quy trình đảm bảo tính ổn định, độ chính xác trên 95%.Giới hạn phát hiện (LOD) và giới hạn định lượng (LOQ)tương đương và thấp hơn một số tác giả khác đã nghiên cứu; tiết kiệm được hóa chất và thời gian phân tích.
* Áp dụng quy trình xây dựng được đãphân tích 90 mẫu nước tiểu của 90đối tượng tiếp xúcvới ethylbenzencho thấy có 34,44% đối tượng có nồng độPGAniệu vượt quá nồng độ tương ứng quá giới hạn cho phép của ethylbenzen trong môi trường.
4.2. Kiến nghị
Áp dụng rộng rãi kỹ thuật xác định PGA trong nước tiểu để làm công cụ giám sát sinh học cho người lao động có tiếp xúc với ethylbenzen.
TÀI LIỆU THAM KHẢO
[1]. American Conference of Governmental Industrial Hygienists. (2007), “Etylbenzen. In: Documentation of the Threshold Limit Vales and Biological Exposure Indices”, vol. 7th edition
[2]. Danish Ministry of the Environmental. (2013), “Evaluation of health hazards by exposure to Ethylbenzene and proposal of a health-based quality criterion for ambient air”, p. 12.
[3].Bộ Y tế. (2016), “Thông tư 28/2006/TT- BYT hướng dẫn quản lý bệnh bệnh nghề nghiệp”.
[4]. The Centers for Disease Control and Prevention. (2012), “Laboratory Procedure Manual”. National Center for Environmental Health
[5].Tạ Thị Thảo (2010), Thống kê trong hóa phân tích. Giáo trình môn học,Trường Đại học Khoa học Tự nhiên Đại học Quốc Gia Hà Nôi.
[6]. Viện kiểm nghiện an toàn vệ sinh Thực phẩm Quốc Gia (2010), Thẩm định phương pháp trong phân tích hóa học và vi sinh vật học. NXB Khoa học và Kỹ Thuật.
[7].S. C. Chua, B. L. Lee, L. S. Liau et al. (1993), “Determination of mandelic acid and phenylglyoxylic acid in the urine and its use in monitoring of styrene exposure”, J Anal Toxicol, vol. 17, no. 3, pp. 129-32.
[8]. SW Cui, XF Pan, and HF Yan. (2017), “Determination of phenylglyoxylic acid and mandelic acid in urine by high performance liquid chromatography method”, Zhonghua lao dong wei sheng zhi ye bing za zhi= Zhonghua laodong weisheng zhiyebing zazhi= Chinese journal of industrial hygiene and occupational diseases, vol. 35, no. 10, pp. 774-776.
[9].Udo Knecht, Antje Reske, and Hans-Joachim Woitowitz. (2000), “Biological monitoring of standardized exposure to ethylbenzene: evaluation of a biological tolerance (BAT) value”, Archives of toxicology, vol. 73, no. 12, pp. 632-640.
Nguyễn Thị Hiền, Tống Thị Ngân, Nguyễn Thị Điềm, Đỗ Thị Cẩm Nhung, Vũ Xuân Trung
Viện KH An toàn và Vệ sinh lao động
(Tạp chí HĐKHCN An toàn – Sức khỏe và Môi trường lao động – Số 1,2&3/2019)
(Nguồn tin: Vnniosh.vn)
